

 .
. ;(2)CaCO3+2HCl═CaCl2+H2O+CO2↑;(3)鹽酸濃度太大或澄清石灰水變質等(合理即可).
;(2)CaCO3+2HCl═CaCl2+H2O+CO2↑;(3)鹽酸濃度太大或澄清石灰水變質等(合理即可).

 閱讀快車系列答案
閱讀快車系列答案科目:初中化學 來源: 題型:
 (2013?哈爾濱)如圖是某同學正在繪制的實驗室制取氧氣的裝置圖.請回答下列問題:
(2013?哈爾濱)如圖是某同學正在繪制的實驗室制取氧氣的裝置圖.請回答下列問題:
| ||
| ||
查看答案和解析>>
科目:初中化學 來源: 題型:
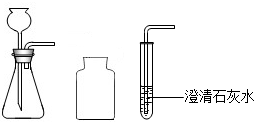
查看答案和解析>>
科目:初中化學 來源: 題型:
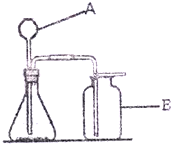 如圖是某同學正在繪制的實驗室制取二氧化碳的裝置圖,請回答下列問題:
如圖是某同學正在繪制的實驗室制取二氧化碳的裝置圖,請回答下列問題:查看答案和解析>>
科目:初中化學 來源:2013年黑龍江省哈爾濱市中考化學試卷(解析版) 題型:填空題
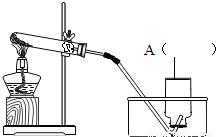
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com