
| 實驗 | 現象 | 化學方程式 |
| 鋁絲插入硫酸銅溶液中 | ||
| 銅絲插入硝酸銀溶液中 | ||
| 銅絲插入硫酸鋁溶液中 |
分析 根據將鋁絲浸入硫酸銅溶液中、銅絲浸入硝酸銀溶液中、銅絲浸入硫酸鋁溶液中的反應現象,判斷能否發生反應,進而可確定三種金屬活動性由強到弱的順序.
解答 解:
將鋁絲浸入硫酸銅溶液中,鋁絲表面有紅色物質析出,溶液變為無色,鋁與硫酸銅溶液反應生成硫酸鋁溶液和銅,說明鋁的金屬活動性比銅強,即鋁>銅,反應的化學方程式為:2Al+3CuSO4=3Cu+Al2(SO4)3.
將銅絲浸入硝酸銀溶液中,銅絲表面有銀白色物質析出,溶液變為藍色,銅與硝酸銀溶液反應生成硝酸銅溶液和銀,說明銅的金屬活動性比銀強,即銅>銀,反應的化學方程式為:Cu+2AgNO3=2Ag+Cu(NO3)2.
將銅絲浸入硫酸鋁溶液中,無明顯變化,說明銅的金屬活動性比鋁弱,即鋁>銅.
鋁>銅,銅>銀,鋁>銅,則三種金屬的活動性順序為鋁>銅>銀.
故答案為:
| 實驗步驟 | 現象 | 反應的化學方程式 |
| 將鋁絲浸入硫酸銅溶液中 | 鋁絲表面有紅色物質析出,溶液變為無色 | 2Al+3CuSO4=3Cu+Al2(SO4)3 |
| 將銅絲浸入硝酸銀溶液中 | 銅絲表面有銀白色物質析出,溶液變為藍色 | Cu+2AgNO3=2Ag+Cu(NO3)2 |
| 將銅絲浸入硫酸鋁溶液中 | 無明顯現象 | / |
點評 本題難度不大,考查了金屬活動性順序的應用,掌握金屬活動性順序并能靈活運用是正確解答此類題的關鍵所在.


科目:初中化學 來源: 題型:選擇題
| A. | 變大 | B. | 不變 | C. | 變小 | D. | 無法判斷 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
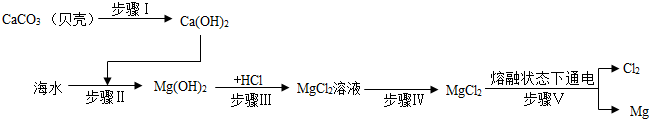
| A. | 步驟Ⅰ通過一步反應即可實現 | |
| B. | 步驟Ⅱ、Ⅲ、Ⅳ的目的是從海水中提純氯化鎂 | |
| C. | 步驟Ⅴ中化學能轉化為電能 | |
| D. | 在此流程中涉及的基本反應類型有4種 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| 選項 | 物質(括號內為雜質) | 試劑 |
| A | FeSO4溶液(CuSO4) | 過量鐵粉 |
| B | CO2氣體(CO) | 氫氧化鈉溶液 |
| C | CaO固體(CaCO3) | 稀鹽酸 |
| D | NaCl溶液(Na2CO3) | 過量氯化鈣溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 綠原酸屬于有機高分子 | |
| B. | 綠原酸由碳、氧三種元素質量比為16:9 | |
| C. | 綠原酸的相對分子質量為354 | |
| D. | 綠原酸中氧元素的質量分數最大 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com