
分析 (1)利用一定量溶液中溶質的質量=溶液質量×溶液中溶質的質量分數,由溶液質量100g和溶液的溶質質量分數15%,計算溶液中溶質的質量;
(2)加入水后溶液質量增大而溶質質量不變,利用溶液中溶質的質量分數的計算公式,計算加水后所得溶液的溶質質量分數.
(3)配制過程中溶質質量不變;由稀溶液的溶液質量和溶質質量分數可以計算出溶質質量,由溶質質量和濃溶液的溶質質量分數可以計算出濃溶液的質量,并據溶液的質量=溶液的密度×溶液的體積分析解答.
解答 解:(1)100g溶質質量分數為15%過氧乙酸溶液中含溶質的質量:100g×15%=15g,答:100g過氧乙酸溶液中含溶質為15g;
(2)向100g該溶液中加入200g水,所得溶液的溶質質量分數=$\frac{15g}{100g+200g}$×100%=5%.
答:所得溶液的溶質的質量分數為5%.
(3)要配制的過氧乙酸溶液中含有過氧乙酸的質量為:100g×5%=5g
設需要質量分數為15%過氧乙酸溶液的質量為x,則
x×15%=5g
x=33.3g
則需要加水100-33.3=66.7mL
答:需要15%的過氧乙酸溶液33.3g,需要加水66.7毫升.
點評 根據溶液中溶質的質量分數=$\frac{溶質的質量}{溶液的質量}$×100%,若已知等式中任意兩個量可計算第三個量.


 中考利劍中考試卷匯編系列答案
中考利劍中考試卷匯編系列答案 教育世家狀元卷系列答案
教育世家狀元卷系列答案 黃岡課堂作業本系列答案
黃岡課堂作業本系列答案 單元加期末復習先鋒大考卷系列答案
單元加期末復習先鋒大考卷系列答案科目:初中化學 來源: 題型:實驗探究題
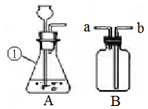 通過近一年的化學學習,你已經掌握了實驗室制取氣體的有關方法.請根據下圖回答問題:
通過近一年的化學學習,你已經掌握了實驗室制取氣體的有關方法.請根據下圖回答問題:查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
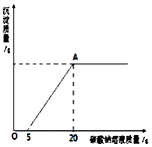 為了探究石灰石與稀鹽酸反應制備二氧化碳后的廢液中的溶質成分,將廢液過濾,取濾液20g于燒杯中,在不斷振蕩的條件下,向其中滴加質量分數為10.6%的碳酸鈉溶液直至過量,有關的變化如圖所示:根據題中有關信息和圖象分析回答下列問題
為了探究石灰石與稀鹽酸反應制備二氧化碳后的廢液中的溶質成分,將廢液過濾,取濾液20g于燒杯中,在不斷振蕩的條件下,向其中滴加質量分數為10.6%的碳酸鈉溶液直至過量,有關的變化如圖所示:根據題中有關信息和圖象分析回答下列問題查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 碳酸鈣 $\stackrel{高溫}{→}$氧化鈣+二氧化碳 | |
| B. | 紅磷+氧氣$\stackrel{點燃}{→}$ 五氧化二磷 | |
| C. | 石蠟+氧氣$\stackrel{點燃}{→}$ 二氧化碳+水 | |
| D. | 氯酸鉀$→_{加熱}^{二氧化錳}$氯化鉀+氧氣 |
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
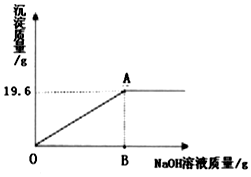 有一包固體粉末,可能是碳酸鈣、硫酸鈉、硫酸銅、碳酸鈉中的一種或多種.某實驗小組對其成分進行了探究活動.
有一包固體粉末,可能是碳酸鈣、硫酸鈉、硫酸銅、碳酸鈉中的一種或多種.某實驗小組對其成分進行了探究活動. 查看答案和解析>>
科目:初中化學 來源: 題型:解答題
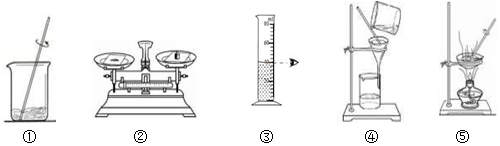
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
| ①實驗操作 | ②實驗現象 |
| 剪下一片變黑的銅片,放入試管中,加入足量的稀硫酸溶液 | 銅片表面的黑色物質全部消失,露出紅色的銅,溶液變為藍色 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com