
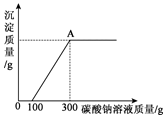
 為了探究石灰石與稀鹽酸反應制備二氧化碳后的廢液中的溶質成分,將廢液過濾,取濾液224.4克于燒杯中,在不斷振蕩的條件下,向其中逐滴加質量分數為10.6%的碳酸鈉溶液直至過量,有關的變化如圖所示.經測定A中只含有一種溶質.根據題中有關信息和圖象分析回答下列問題.
為了探究石灰石與稀鹽酸反應制備二氧化碳后的廢液中的溶質成分,將廢液過濾,取濾液224.4克于燒杯中,在不斷振蕩的條件下,向其中逐滴加質量分數為10.6%的碳酸鈉溶液直至過量,有關的變化如圖所示.經測定A中只含有一種溶質.根據題中有關信息和圖象分析回答下列問題.分析 (1)根據石灰石與鹽酸反應后的廢液中一定含有溶質氯化鈣,加入碳酸鈉開始沒有沉淀生成,說明廢液中含有多余的鹽酸進行分析;
(2)根據碳酸鈉溶液的質量和溶質質量分數計算碳酸鈉的質量,然后計算鈉元素的質量分數;
(3)根據A點處溶液中溶質氯化鈉中的鈉元素完全來自于碳酸鈉中的鈉元素,碳酸鈉溶液的質量和溶質質量分數可以計算鈉元素的質量,進一步可以計算氯化鈉的質量,從而可以計算A點處溶液中溶質的質量分數.
解答 解:(1)石灰石與鹽酸反應后的廢液中一定含有溶質氯化鈣,加入碳酸鈉開始沒有沉淀生成,說明廢液中含有多余的鹽酸,所以含有的溶質有CaCl2,HCl;
(2)碳酸鈉溶液中鈉元素的質量分數為:$\frac{300g×10.6%×\frac{46}{106}}{300g}$=4.6%;
(3)設A點處溶液中溶質氯化鈉的質量為y,
由Na2CO3+2HCl═2NaCl+H2O+CO2↑,Na2CO3+CaCl2═CaCO3↓+2NaCl 可知,
Na2CO3~2NaCl,
106 117
300g×10.6% y
$\frac{106}{300g×10.6%}$=$\frac{117}{y}$
y=35.1g
設生成沉淀的質量為x
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100
200g×10.6% x
$\frac{106}{200g×10.6%}$=$\frac{100}{x}$
x=20g
設碳酸鈉和稀鹽酸反應生成二氧化碳的質量為z,
Na2CO3+2HCl═2NaCl+H2O+CO2↑,
106 44
100g×10.6% z
$\frac{106}{100g×10.6%}$=$\frac{44}{z}$
z=4.4g
A點處溶液中溶質的質量分數為:$\frac{35.1g}{224.4g+300g-20g-4.4g}$×100%=7.0%.
答:A點處溶液中溶質的質量分數為6.1%.
故答案為:(1)CaCl2,HCl;
(2)4.6%;
(3)7.0%.
點評 本題主要考查學生運用假設法和化學方程式進行計算和推斷的能力,同時考查了分析數據的能力,計算時要注意規范性和準確性.


科目:初中化學 來源: 題型:選擇題
| A. | 血液,pH為7.35~7.45 | B. | 胃液,pH為0.8~1.5 | ||
| C. | 牛奶,pH為6.3~6.6 | D. | 蘋果汁,pH為2.9~3.3 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | NaOH (Na2CO3):鹽酸 | B. | CO2 (O2):灼熱的銅粉 | ||
| C. | CO (CO2):氫氧化鈉溶液 | D. | O2 (H2O):濃硫酸 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題

查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
查看答案和解析>>
科目:初中化學 來源: 題型:多選題
| A. | 用10mL量筒量取10mL水 | |
| B. | 為了加快過濾速度,用玻璃棒攪動過濾器里的液體 | |
| C. | 稀釋濃硫酸時,應將濃硫酸慢慢加入水中,并用玻璃棒不斷攪拌 | |
| D. | 實驗室用排水法收集氣體時,一有氣泡冒出馬上收集,以免造成浪費 | |
| E. | 切忌向燃著的酒精燈內添加酒精,可以用燃著的酒精燈去點燃另一盞酒精燈 | |
| F. | 取用液體藥品時,要把瓶塞倒放在桌面上,標簽朝向手心,放回原處時標簽向外 | |
| G. | 為了測定溶液的酸堿度,可以選擇紫色石蕊試液進行檢驗 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題

查看答案和解析>>
科目:初中化學 來源: 題型:計算題
 為測定某鐵粉樣品(含少量木炭粉)中鐵的含量,往盛有219g稀鹽酸的燒杯中不斷加入鐵粉樣品,測得生成氫氣的質量與所加鐵粉樣品的質量關系如圖所示.
為測定某鐵粉樣品(含少量木炭粉)中鐵的含量,往盛有219g稀鹽酸的燒杯中不斷加入鐵粉樣品,測得生成氫氣的質量與所加鐵粉樣品的質量關系如圖所示.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com