
 酸、堿、鹽是重要的化合物,研究它們的性質有重要意義.
酸、堿、鹽是重要的化合物,研究它們的性質有重要意義.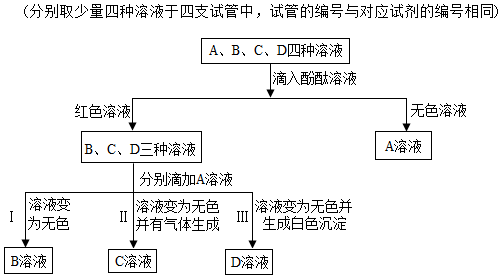
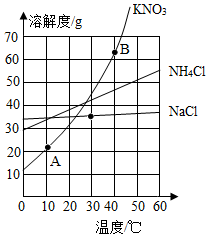
分析 (1)根據固體的溶解度曲線可以:①查出某物質在一定溫度下的溶解度,從而確定物質的溶解性,②比較不同物質在同一溫度下的溶解度大小,從而判斷飽和溶液中溶質的質量分數的大小,③判斷物質的溶解度隨溫度變化的變化情況,從而判斷通過降溫結晶還是蒸發結晶的方法達到提純物質的目的;
(2)根據氫氧化鈉、氫氧化鉀屬于堿,碳酸鈉溶液顯堿性,能使酚酞變紅色,碳酸鹽會與鋇離子反應生成碳酸鋇沉淀,會與酸反應生成二氧化碳氣體等知識進行分析.
解答 解:(1)①通過分析溶解度曲線可知,三種固體物質的溶解度受溫度影響最小的是氯化鈉;
②30℃時,硝酸鉀的溶解度最大,氯化銨次之,氯化鈉的溶解度最小,所以三種固體物質飽和水溶液中溶質的質量分數由大到小的順序是:硝酸鉀、氯化銨、氯化鈉;
③圖中A、B點的坐標為:A(10,21)、B(40,64),
設40℃100g硝酸鉀飽和溶液中溶質質量為x
100:x=(100g+64g):64g
x=39g
所以溶劑質量為:100g-39g=61g,
設61g水在10℃時最多溶解硝酸鉀的質量為y
100:21=61:y
y=12.81g
所以析出KNO3固體的質量為:39g-12.8g=26.2g;
(2)A、B、C、D四種溶液中滴入酚酞,A溶液顯無色,所以A是稀硫酸,B、C、D是氫氧化鋇、氫氧化鈉、碳酸鈉中的一種,滴加稀硫酸,C溶液變為無色,有氣泡產生,所以C是碳酸鈉,D溶液變為無色,并產生白色沉淀,所以D是氫氧化鋇,B溶液變為無色,所以B是氫氧化鈉,所以
①反應Ⅲ是氫氧化鋇和硫酸反應生成硫酸鋇沉淀和水,化學方程式為:Ba(OH)2+H2SO4=BaSO4↓+2H2O;
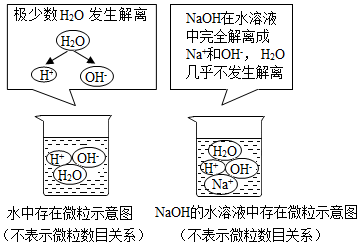
②通過分析題中的微觀圖示,水中含有氫離子和氫氧根離子,水顯中性;氫氧化鈉溶液中含有鈉離子、氫氧根離子、氫離子,所以C溶液能使酚酞溶液變紅的原因是氫氧根離子的數目大于氫離子的數目,故選:d.
故答案為:(1)①氯化鈉;
②硝酸鉀、氯化銨、氯化鈉;
③26.2;
(2)①Ba(OH)2+H2SO4=BaSO4↓+2H2O;
②d.
點評 本題難度不是很大,主要考查了固體的溶解度曲線所表示的意義,及根據固體的溶解度曲線來解決相關的問題,從而培養分析問題、解決問題的能力.


科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 除去鐵制品表面的鐵銹,用過量的稀硫酸長時間浸泡 | |
| B. | 驗證甲烷中含有H2,點燃,在火焰上方罩一只干冷燒杯,觀察內壁是否出現液滴 | |
| C. | 鑒別化肥KNO3和NH4Cl,取樣與熟石灰混合研磨,聞氣味 | |
| D. | 檢驗NaOH是否變質,取樣,加水溶解后滴加酚酞試液,觀察溶液顏色是否變紅 |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
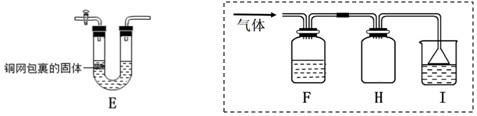
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com