
| FeCl3溶液 | FeSO4溶液 | |
| 滴入NaOH溶液的現象 | 生成紅褐色沉淀 | 先生成白色絮狀沉淀,迅速變成灰綠色,最后變成紅褐色沉淀. |
化學方程式 | FeCl3+3NaOH=Fe(OH)3↓+3NaCl 基本反應類型屬于 復分解反應反應. | FeSO4+2NaOH=Fe(OH)2↓+Na2SO4 Fe(OH)2+O2+H2O=Fe(OH)3 (用化學式填寫空白,不需配平) |
分析 (1)根據鹽和堿的性質,可寫出FeCl3溶液和NaOH溶液反應的方程式,并由反應物、生成物的種類和反應的特點判定反應的類型;
(2)根據鹽和堿的性質,FeSO4溶液中滴入NaOH溶液,先生成白色絮狀沉淀是氫氧化亞鐵,根據反應的現象和質量守恒定律可完成并配平氫氧化亞鐵轉化成氫氧化鐵的方程式;
(3)單質的C可以將CO2還原為CO,單質的鐵也可以將FeCl3還原成FeCl2.
解答 解:【實驗過程】(1)FeCl3溶液和NaOH溶液反應的方程式:FeCl3+3NaOH=Fe(OH)3↓+3NaCl,此反應屬于復分解反應;
(2)FeSO4溶液滴入NaOH溶液,生成白色絮狀沉淀是氫氧化亞鐵沉淀,白色氫氧化亞鐵在水中不穩定,容易跟水中的氧氣反應生成紅棕色的氫氧化鐵.由于氫氧化亞鐵有少量溶于水中,亞鐵離子顯綠色,所以溶液呈綠色,同時也會轉化成黃色的鐵離子,灰色就是白色、紅棕、綠色、黃色的混合色.在加上這種轉化是有時間過程的,所以隨著各種離子含量變化,顏色變化就由此而來了.最后變成紅褐色沉淀是氫氧化鐵沉淀,根據質量守恒定律完成并配平反應的方程式,4Fe(OH)2+O2+2H2O=4Fe(OH)3;
【反思交流】
(1)氫氧化亞鐵是白色而不是淺綠色.
(2)根據CO2與C的反應,要讓FeCl3溶液可以轉化為FeCl2溶液,所以,小軍的理由是:單質的鐵也可以將FeCl3還原成FeCl2.
故答案為:FeCl3+3NaOH=Fe(OH)3↓+3NaCl;復分解;4;O2;Fe(OH)3,即:
| FeCl3溶液 | FeSO4溶液 | |
| 滴入NaOH溶液的現象 | ||
化學方程式 | FeCl3+3NaOH=Fe(OH)3↓+3NaCl 基本反應類型屬于 復分解反應. | FeSO4+2NaOH=Fe(OH)2↓+Na2SO4 Fe(OH)2+O2+H2O=Fe(OH)3 |
點評 本題不僅考查了鹽和堿的性質、反應的現象,同時還考查了學生知識與信息的遷移運用能力.


科目:初中化學 來源: 題型:選擇題
| A. | 活性炭、木炭都具吸附性 | |
| B. | 一氧化碳和二氧化碳都有毒 | |
| C. | 木炭、一氧化碳在一定條件下都能與氧化銅反應 | |
| D. | 金剛石、石墨和C60都是碳元素的單質 |
查看答案和解析>>
科目:初中化學 來源: 題型:推斷題

查看答案和解析>>
科目:初中化學 來源: 題型:解答題

查看答案和解析>>
科目:初中化學 來源: 題型:填空題
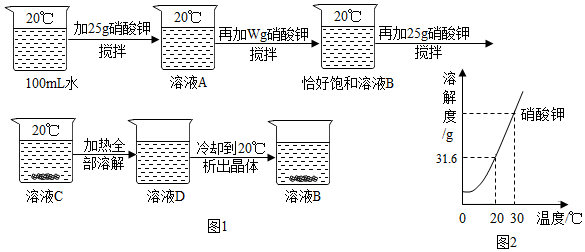
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
| 實驗編號 | 實驗藥品 | 分解溫度(℃) |
| ① | KClO3 | 580 |
| ② | KClO3、MnO2(質量比1:1) | 350 |
| ③ | KClO3、CuO(質量比1:1) | 370 |
| ④ | KClO3、Fe2O3(質量比1:1) | 390 |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
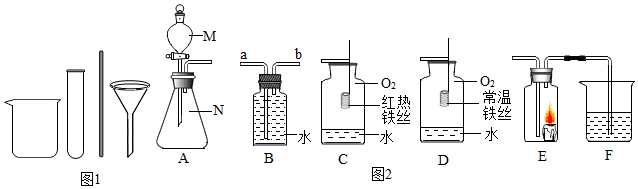
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
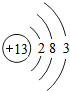 是鋁的原子結構示意圖.下列說法不正確的是C.
是鋁的原子結構示意圖.下列說法不正確的是C.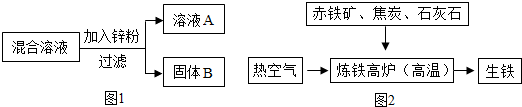
| 實驗步驟 | 現象 | 有關反應的化學方程式 |
| 取少量固體B, 滴加稀鹽酸 | 有氣泡 產生 | Zn+2HCl=ZnCl2+H2↑ |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com