2010年4月17日青海玉樹發生地震.為了防止災區的病菌傳播,防疫人員大量使用了“漂白粉”來殺菌消毒.“漂白粉”的有效成分為次氯酸鈣[化學式為:Ca(ClO)2].請回答:
(1)次氯酸鈣中鈣、氯、氧三種元素的質量比為________.
(2)次氯酸鈣中氯元素的質量分數是________.(精確到0.1%)
(3)若災區飲用水需要5%漂白粉溶液250g來消毒,則需要20%的漂白粉溶液________g.
解:(1)化合物中元素的質量比是元素的相對原子質量與原子個數的乘積之比.
因此次氯酸鈣中鈣、氯、氧三種元素的質量比為40:35.5×2:16×2=40:71:32.
(2)化合物中元素的質量分數是化學式中元素的相對原子質量與原子個數的乘積跟相對分子質量之比.
因此次氯酸鈣中氯元素的質量分數為
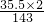
×100%≈49.7%.
(3)溶液在進行稀釋的過程中,溶質的質量不變.
因此需要20%的漂白粉溶液的質量為250g×5%÷20%=62.5g
故答案為:
(1)40:71:32
(2)49.7%
(3)62.5
分析:只有熟悉化學式的意義、有關化學式的計算方法和有關溶質質量分數的計算方法,才能得出本題的正確答案.
點評:本題主要考查化學式的意義、有關化學式的計算方法和有關溶質質量分數的計算方法,難度稍大.

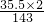 ×100%≈49.7%.
×100%≈49.7%.
