【答案】
分析:(一)猜想與假設:根據碳酸鈉在水中水解的產物進行分析.
(三)設計與實驗:
(1)根據過濾能除去不溶性雜質進行解答;
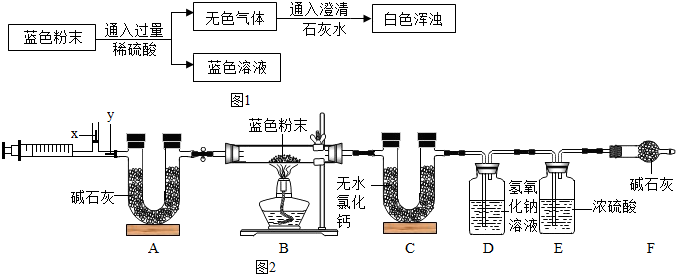
(2)根據碳酸鈉會與鹽酸反應生成二氧化碳進行分析;
(3)根據氫氧化鈣會與二氧化碳反應生成碳酸鈣沉淀進行分析;
(4)根據無水硫酸銅遇水變藍進行分析;
(5)根據檢驗水要放在檢驗二氧化碳的前面進行分析;
(6)根據氫氧化銅和碳酸銅的分解溫度進行分析;根據氫氧化銅和碳酸銅分解的化學方程式進行分析.
(7)剩余固體加熱到更高溫度固體的質量又會減少,根據氧化銅中所含的兩種元素可猜想可能是氧化銅中的氧元素轉化為氧氣,根據計算會發現氧化銅中氧元素的質量大于固體減少的質量,那么就可能是氧化銅中的部分氧元素轉化為氧氣.
解答:解:(一)猜想與假設:碳酸鈉是強堿弱酸鹽,在水中水解后會生成氫氧根離子;故答案為:堿;
(三)設計與實驗:
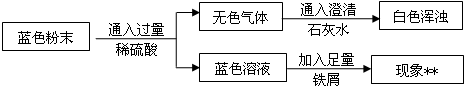
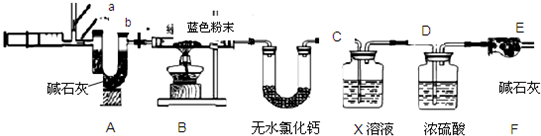
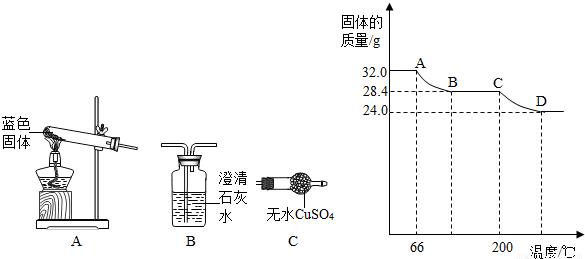
(1)過濾能除去不溶性雜質,將反應后的固、液混合物經過濾、洗滌、低溫烘干得藍色固體;故答案為:過濾;
(2)固體上殘留的碳酸鈉會與鹽酸反應生成二氧化碳氣體;故答案為:取最后洗滌液少量,滴加適量的稀鹽酸,無氣泡產生;
(3)B中無現象,說明沒有生成二氧化碳,也就說明固體中沒有碳酸銅,故答案為:二;
(4)檢驗水要放在檢驗二氧化碳的前面,否則通過石灰水時攜帶的水蒸氣會對檢驗水產生干擾,實驗中:B中的現象為澄清石灰水變渾濁,C中白色固體變藍色;故答案為:C;B;澄清石灰水變渾濁;
(5)AB段的溫度大于60℃但是沒有超過200℃,從圖象中看出也不超過100℃,符合氫氧化鐵的分解溫度,故答案為:Cu(OH)
2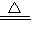
CuO+H
2O;
CD段的溫度超過了200℃,符合碳酸銅的分解溫度,故答案為:CuCO
3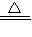
CuO+CO
2↑;
(6)AB段是氫氧化銅在分解,固體質量減少3.6克,CD段是碳酸銅在分解,固體質量減少4.4克,
Cu(OH)
2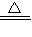
CuO+H
2O CuCO
3
CuO+CO
2↑
從方程式可以看出一個氫氧化銅分解會生成一個水,一個碳酸銅分解會產生一個二氧化碳,而AB段的氫氧化銅減少了3.6克水,減少了0.2個水,需要0.2克氫氧化銅,CD段的碳酸銅分解減少了4.4克二氧化碳,相當于減少了0.1個二氧化碳,需要0.1個碳酸銅,所以a:b=2:1;故答案為:a:b=2:1;
(7)氧化銅加熱后質量又會減少,應該是氧化銅中的氧元素轉化為氧氣,24g氧化銅的氧元素的質量=24g×
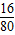
=4.8g,大于2.4g,說明是氧化銅中的部分氧元素轉化為氧氣.
故答案為:4CuO
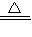
2Cu
2O+O
2↑.
點評:在解此類題時,首先要將題中的知識認知透,然后結合學過的知識進行解答,此類題難度較大,要細心進行分析解答.

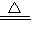 CuO+H2O;
CuO+H2O;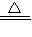 CuO+CO2↑;
CuO+CO2↑;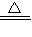 CuO+H2O CuCO3
CuO+H2O CuCO3 CuO+CO2↑
CuO+CO2↑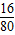 =4.8g,大于2.4g,說明是氧化銅中的部分氧元素轉化為氧氣.
=4.8g,大于2.4g,說明是氧化銅中的部分氧元素轉化為氧氣.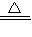 2Cu2O+O2↑.
2Cu2O+O2↑.