考點:原子結構示意圖與離子結構示意圖,元素周期表的特點及其應用,化學符號及其周圍數字的意義
專題:化學用語和質量守恒定律
分析:(1)原子中,質子數=核外電子數.
(2)根據元素的化學性質跟它的原子的最外層電子數目關系非常密切,最外層電子數相同的元素化學性質相似,據此進行分析解答.
(3)M元素最外層電子數是1,在化學反應中易失去1個電子而形成陽離子.
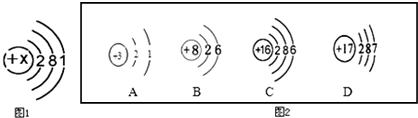
(4)圖2中的D元素的核內質子數為17,為氯元素,據此進行分析判斷.
解答:解:(1)原子中,質子數=核外電子數,由M原子結構示意圖:該原子中X=2+8+1=11.
(2)元素的化學性質跟它的原子的最外層電子數目關系非常密切,最外層電子數相同的元素化學性質相似,M元素的最外層電子數為1,A中最外層電子數也為1,最外層電子數相同,化學性質最相似.
(3)M元素核內質子數為11,為鈉元素;其最外層電子數是1,在化學反應中易失去1個電子,形成帶1個單位正電荷的M離子,其離子符號為:Na+.
(4)M元素為鈉元素,圖2中的D元素的核內質子數為17,為氯元素,鈉元素顯+1價,氯元素顯-1價,形成化合物的化學式為NaCl.
故答案為:(1)11;(2)A;(3)Na+;(4)NaCl.
點評:本題難度不大,考查學生對原子結構示意圖及其意義的理解,了解原子結構示意圖的意義是正確解題的關鍵.



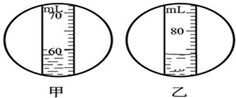 15.4gNaCl完全溶解在如圖甲所示的水中,將完全溶解后所得溶液全部倒入原量筒中,液面位置如圖乙,則所得NaCl溶液的密度為
15.4gNaCl完全溶解在如圖甲所示的水中,將完全溶解后所得溶液全部倒入原量筒中,液面位置如圖乙,則所得NaCl溶液的密度為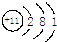 ,該原子在化學反應中易
,該原子在化學反應中易