
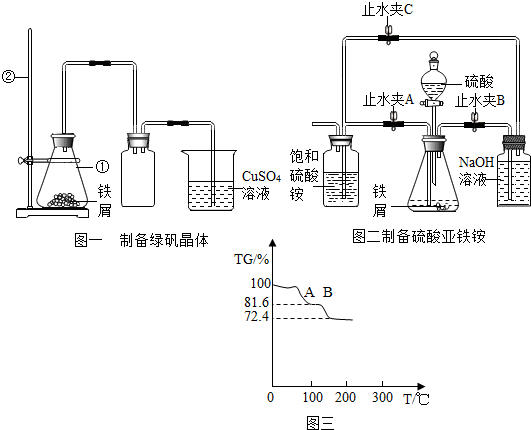
分析 (1)根據實驗室常用儀器的名稱和題中所指儀器的作用進行分析;
(2)根據制備硫酸亞鐵銨,需要硫酸亞鐵,和硫酸銨,左邊的集氣瓶中已經有了硫酸銨,需要利用中間的錐形瓶制備硫酸亞鐵,需要通過分液漏斗滴加硫酸,稀硫酸和硫化亞鐵生成硫酸亞鐵和硫化氫,燒杯中的氫離子濃度不變進行分析;
(3)①根據實驗操作和注意事項確定氫氣和氫氧化鈉的作用,氫氧化鈉和硫化氫反應生成硫化鈉和水進行分析;
②據制備硫酸亞鐵銨,需要硫酸亞鐵,和硫酸銨,左邊的集氣瓶中已經有了硫酸銨,需要利用中間的錐形瓶制備硫酸亞鐵,需要通過分液漏斗滴加硫酸,結合裝置中的反應原理分析關閉和打開活塞的順序;
(4)根據題中的提示和圖象的變化趨勢進行分析.對硫酸亞鐵銨[FeSO4•(NH4)2SO4•6H2O]樣品進行加熱到100℃時,首先是固體表面的分子水蒸發(fā)得到硫酸亞鐵銨[FeSO4•(NH4)2SO4•6H2O],這一步是物理變化,繼續(xù)加熱到100-200℃時,已知200℃以前只有結晶水失去,因此硫酸亞鐵銨[FeSO4•(NH4)2SO4•6H2O]中的結晶水開始脫去,這一步是化學變化.
解答 解:(1)通過分析題中所指儀器的作用可知,①是錐形瓶,②是鐵架臺;
(2)通過分析可知,圖一中儀器①盛放的液體是稀硫酸,廣口瓶的作用是暫時儲存硫化氫,稀硫酸和硫化亞鐵生成硫酸亞鐵和硫化氫,化學方程式為:FeS+H2SO4=FeSO4+H2S↑,燒杯中的氫離子濃度不變,所以燒杯中溶液的pH將隨著反應的進行不變;
(3)①氫氧化鈉和硫化氫反應生成硫化鈉和水,化學方程式為:2NaOH+H2S=Na2S+2H2O,氫氣的作用是:①排盡整個裝置中的空氣,防止FeSO4被氧化 ②將硫酸亞鐵溶液壓入飽和碳酸銨溶液;
②待錐形瓶中的鐵屑快反應完時,關閉止水夾BC,打開止水夾A;
(4)通過分析可知,對硫酸亞鐵銨[FeSO4•(NH4)2SO4•6H2O]樣品進行加熱到100℃時,首先是固體表面的分子水蒸發(fā)得到硫酸亞鐵銨[FeSO4•(NH4)2SO4•6H2O],這一步是物理變化,繼續(xù)加熱到100-200℃時,已知200℃以前只有結晶水失去,因此硫酸亞鐵銨[FeSO4•(NH4)2SO4•6H2O]中的結晶水開始脫去,這一步是化學變化.
所以TG%從100%降低為72.4%時,發(fā)生反應的化學方程式是:FeSO4•(NH4)2SO4•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$FeSO4(NH4)2SO4+6H2O;
假設硫酸亞鐵銨晶體質量是392克,加熱到200℃時,失去結晶水,剩下的硫酸亞鐵銨質量為:392g×$\frac{284}{392}$=284g,固體質量分數(shù)減少為:$\frac{284g}{392g}$×100%=72.4%,所以AB段物質的化學式為:FeSO4•(NH4)2SO4.
故答案為:(1)錐形瓶,鐵架臺;
(2)稀硫酸,暫時儲存硫化氫,F(xiàn)eS+H2SO4=FeSO4+H2S↑,不變;
(3)①2NaOH+H2S=Na2S+2H2O,①排盡整個裝置中的空氣,防止FeSO4被氧化 ②將硫酸亞鐵溶液壓入飽和碳酸銨溶液;
②BC,A;
(4)FeSO4•(NH4)2SO4•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$FeSO4(NH4)2SO4+6H2O;
FeSO4•(NH4)2SO4.
點評 本題的難度比較大,閱讀量多,在做這類題時,對題意要理解透,找出有用的物質,然后根據問題結合所學的知識進行解答.


 浙大優(yōu)學小學年級銜接捷徑浙江大學出版社系列答案
浙大優(yōu)學小學年級銜接捷徑浙江大學出版社系列答案科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 將50.0mL酒精與50.0mL蒸餾水混合,所得溶液體積小于100.0mL | |
| B. | 用托盤天平稱取5.62 g 氯化鈉固體 | |
| C. | 石蠟在氧氣中燃燒時,有水和二氧化碳生成 | |
| D. | 硫在空氣中燃燒發(fā)出明亮藍紫色火焰,生成無色無味氣體 |
查看答案和解析>>
科目:初中化學 來源: 題型:多選題
| A. | 食鹽(細沙) | B. | 氯化鉀(二氧化錳) | C. | 大米(細沙) | D. | 鐵粉(硫黃粉) |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題

查看答案和解析>>
科目:初中化學 來源: 題型:解答題
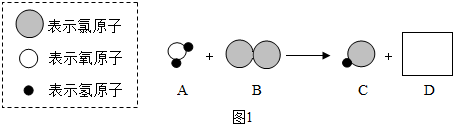

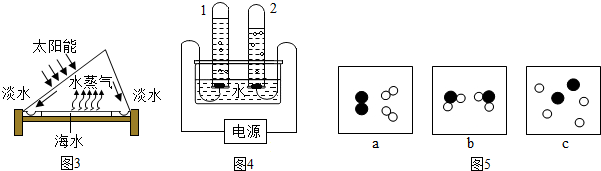
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
 如圖所示裝置可用于測定空氣中氧氣的含量,實驗前在集氣瓶內加入少量水,并做上記號.下列說法中錯誤的是( )
如圖所示裝置可用于測定空氣中氧氣的含量,實驗前在集氣瓶內加入少量水,并做上記號.下列說法中錯誤的是( )| A. | 該實驗證明氧氣約占空氣體積的$\frac{1}{5}$ | |
| B. | 實驗時紅磷一定要足量 | |
| C. | 在實驗過程中,如果紅磷伸入太慢的話,會使實驗結果比實際值偏小 | |
| D. | 紅磷燃燒產生大量的白煙,等火焰熄滅后并冷卻后再打開彈簧夾 |
查看答案和解析>>
湖北省互聯(lián)網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com