
分析 (1)、據復分解反應發生的條件考慮;(2)、【猜想】根據反應的程度進行猜想:恰好反應、一種物質完全反應,另一種物質有剩余;
【進行實驗】根據酚酞遇堿變紅來進行解答;根據鹽酸的性質進行分析,但注意氯化鈣中也含有氯離子;
【反思與拓展】
①根據實驗的結論進行發生反思;
②根據酸會與碳酸鈣反應進行分析③.計算出100g污水中的HCl的質量,然后根據鹽酸和氫氧化鈣反應的化學方程式求出至少需要熟石灰的質量.
解答 解:(1)復分解反應發生的條件是:生成物中有沉淀、水或氣體放出,氫氧化鈣和鹽酸反應生成了氯化鈣和水,故符合條件;
(2)【猜想】反應可能是恰好反應,只有氯化鈣(猜想二)、也可能是一種物質完全反應,另一種物質有剩余,若氫氧化鈣過量,則含有氫氧化鈣和氯化鈣(猜想一);若鹽酸過量,則含有鹽酸和氯化鈣(猜想三);
【進行實驗】因為酚酞遇堿會變紅色,而結論是猜想一不正確,即不含有氫氧化鈣,故觀察到的現象是溶液無明顯變化(或溶液不變紅色);
根據結論猜想二不正確,猜想三正確,即含有鹽酸和氯化鈣,其中的氯化鈣溶液可以和碳酸鈉溶液反應生成沉淀,稀鹽酸和碳酸鈉反應生成二氧化碳氣體,因為碳酸鈣在鹽酸存在的情況下不能以沉淀的形式析出,故碳酸鈉先和鹽酸反應產生氣泡,再和氯化鈣反應產生沉淀;
雖然鹽酸能夠和硝酸銀反應產生沉淀,但由于其中的氯化鈣也能夠和硝酸銀產生相同的現象,不能選擇;
【反思與拓展】
①因為反應可能是完全反應,也可能是其中的一種反應物過量,因此在分析化學反應后所得物質成分時,除考慮生成物外還需考慮反應物的用量;
②鹽酸會與碳酸鈣反應而將過量鹽酸除去.
③解:設至少需要熟石灰的質量為x
污水中HCl的質量:100g×7.3%=7.3g
2HCl+Ca(OH)2═CaCl2+2H2O
73 74
7.3g x
$\frac{73}{7.3g}=\frac{74}{x}$
解之得:x=7.4g
答:至少需要熟石灰7.4g.
故答案為:(1)有水生成;(2)猜想三:可能是CaCl2、HCl;
【進行實驗】溶液無色(或無明顯現象);先產生氣泡,后出現白色沉淀; C;
【反思與拓展】
①反應物是否過量; ②CaCO3;③7.4g.
點評 本題考查了酸堿中和反應以及實驗設計的能力.設計實驗時,可以從反應后的產物和其有關的性質著手;檢驗時要注意氯離子的干擾.


 閱讀快車系列答案
閱讀快車系列答案科目:初中化學 來源: 題型:選擇題
| A. | 酚酞 | B. | BaCl2 | C. | CO2 | D. | AgNO3 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 給燒杯中液體加熱時,在燒杯下面墊上石棉網 | |
| B. | 被加熱的玻璃容器外壁如有水,加熱前應擦干 | |
| C. | 熄滅酒精燈只能用燈帽蓋滅,不能用嘴吹、手扇等方法熄滅 | |
| D. | 用托盤天平稱量物質時,先加小砝碼再依次加較大的砝碼 |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
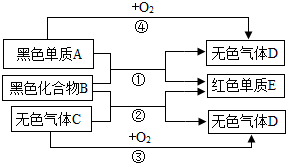 A是非金屬,E是金屬,B、C、D是化合物,它們之間有如下圖所示的轉化關系(反應條件已略去).請回答下列問題:
A是非金屬,E是金屬,B、C、D是化合物,它們之間有如下圖所示的轉化關系(反應條件已略去).請回答下列問題:查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 化學變化和化學反應是同一個概念 | |
| B. | 物質發生化學變化時一定同時發生物理變化 | |
| C. | 化學變化的特征就是有新物質生成 | |
| D. | 有發光放熱等現象的變化一定是化學變化 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 為了節約藥品,將用剩的藥品放回原試劑瓶 | |
| B. | 酒精燈打翻著火,用濕抹布撲蓋 | |
| C. | 玻璃儀器用水沖洗三遍就可以 | |
| D. | 藥品直接放在天平托盤上稱重 |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
 小兵在一本參考書上發現,鎂居然能在二氧化碳氣體中燃燒!于是他迫不及待地做起了這個實驗:將鎂條點燃后迅速伸入盛二氧化碳的集氣瓶中,發現鎂條劇烈燃燒,發出白光,放熱,產生一種白色粉末和一種黑色粉末.
小兵在一本參考書上發現,鎂居然能在二氧化碳氣體中燃燒!于是他迫不及待地做起了這個實驗:將鎂條點燃后迅速伸入盛二氧化碳的集氣瓶中,發現鎂條劇烈燃燒,發出白光,放熱,產生一種白色粉末和一種黑色粉末.查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
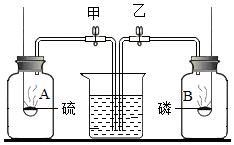 如圖所示,兩個集氣瓶A、B中充滿空氣,氣密性均良好,甲、乙為止水夾,燃燒匙內分別放有足夠的磷和硫粉末.分別點燃紅磷和硫粉,燃燒完全后等集氣瓶冷卻至室溫,同時打開止水夾甲、乙,則燒杯中的水( )
如圖所示,兩個集氣瓶A、B中充滿空氣,氣密性均良好,甲、乙為止水夾,燃燒匙內分別放有足夠的磷和硫粉末.分別點燃紅磷和硫粉,燃燒完全后等集氣瓶冷卻至室溫,同時打開止水夾甲、乙,則燒杯中的水( )| A. | 進入A瓶 | B. | 進入B瓶 | C. | 同時進入A、B兩瓶 | D. | 無任何現象 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com